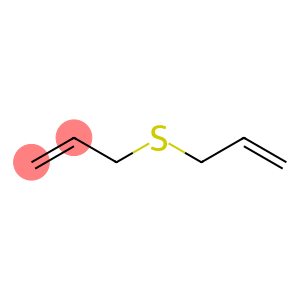
sulfură de alil(CAS#592-88-1)
| Simboluri de pericol | Xi – Iritant |
| Coduri de risc | R10 – Inflamabil R36/37/38 – Iritant pentru ochi, sistemul respirator și piele. |
| Descrierea siguranței | S26 – În caz de contact cu ochii, clătiți imediat cu multă apă și solicitați sfatul medicului. S36 – Purtați îmbrăcăminte de protecție adecvată. S37/39 – Purtați mănuși adecvate și protecție pentru ochi/față S23 – Nu respirați vaporii. S16 – A se păstra departe de surse de aprindere. |
| ID-uri ONU | ONU 1993 3/PG 3 |
| WGK Germania | 2 |
| RTECS | BC4900000 |
| TSCA | Da |
| Cod HS | 29309070 |
| Clasa de pericol | 3 |
| Grup de ambalare | III |
Introducere
Sulfura de alil este un compus organic. Are următoarele proprietăți:
Proprietăți fizice: sulfura de alil este un lichid incolor cu un miros puternic înțepător.
Proprietăți chimice: sulfura de alil este capabilă să reacționeze cu mulți compuși, în special cu reactivi cu electrofilitate, cum ar fi halogeni, acizi, etc. Poate suferi reacții de polimerizare în anumite condiții.
Principalele utilizări ale sulfurei de alil:
Ca intermediar: sulfura de alil poate fi utilizată ca intermediar în sinteza organică și poate participa la o serie de reacții de sinteză organică, de exemplu, poate fi utilizată pentru a sintetiza haloolefine și compuși heterociclici cu oxigen.
Există mai multe metode principale pentru prepararea sulfurei de alil:
Reacția de substituție cu hidrotiol: sulfura de alil poate fi formată prin reacții precum bromura de alil și hidrosulfura de sodiu.
Reacția de conversie a alcoolului alilic: preparată prin reacția alcoolului alilic și acidului sulfuric.
Din punct de vedere al siguranței, sulfura de alil este o substanță iritante care poate provoca iritații și leziuni în contact cu pielea și ochii. Evitați contactul direct cu pielea și ochii atunci când utilizați și mențineți condiții bune de ventilație. Sulfura de alil este volatilă și trebuie evitată pentru expunerea prelungită la concentrații mari de vapori sau gaze.